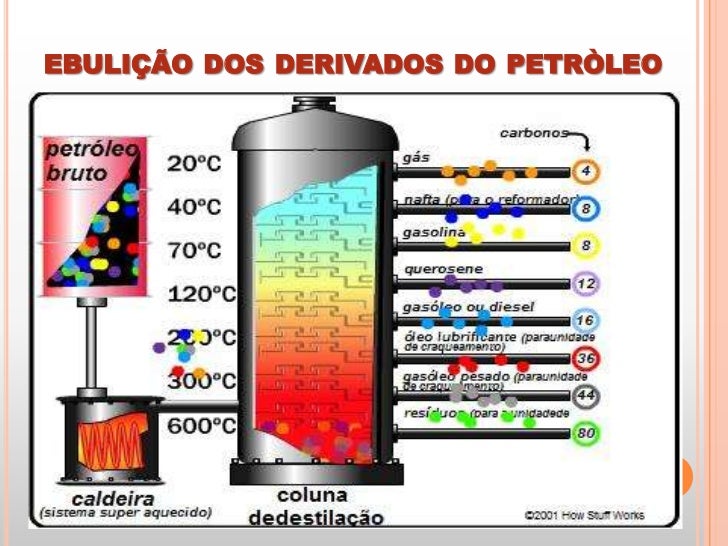
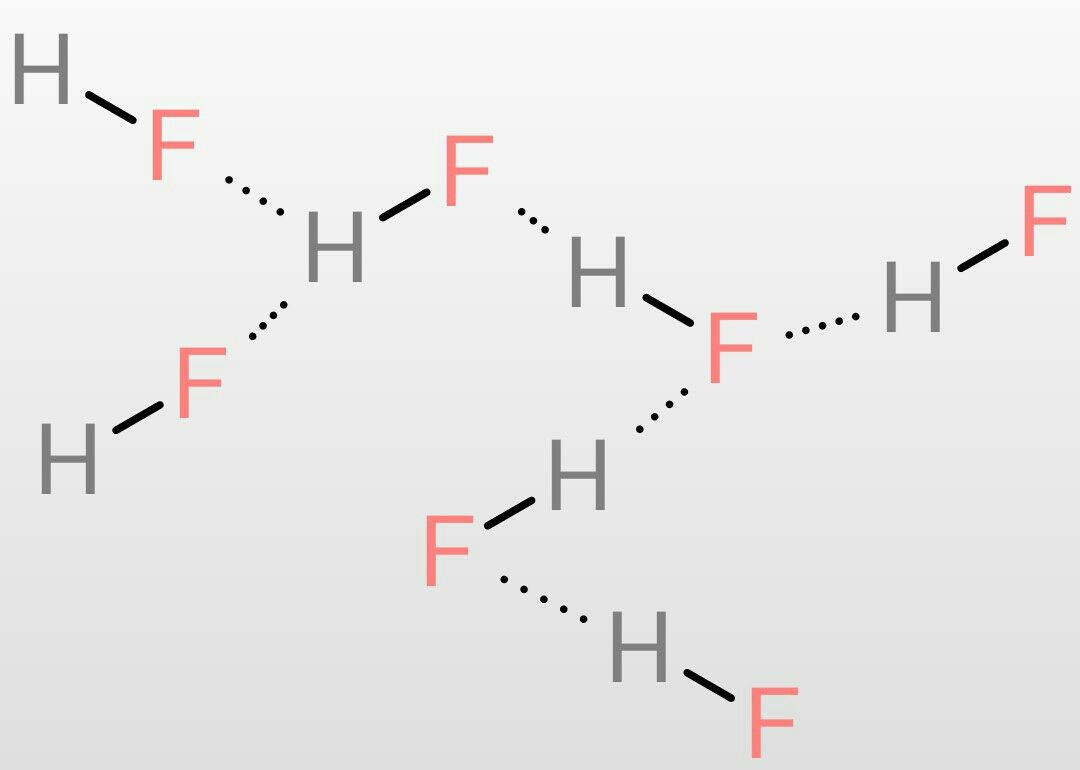
フッ化水素 {HF} 実験的製法} 蛍石 (フッ化カルシウム)に濃}硫酸を加えて\加熱する. CaF2 + 濃 H₂SO₄ 加熱}] CaSO₄ + 2} {HF ^$} 揮発性酸の遊離}) [1zh] 性質}水素結合するため,唯一の弱酸} (← 電離しにくいから})で, {沸点が異常に高い.. hydrogen fluoride. 水素 と フッ素 の 化合物 。 フッ化水素カリウムK HF 2 を熱するか、 蛍石 (ほたるいし) CaF 2 に濃 硫酸 を加えて熱すると得られる。 常温 で 無色 発煙性の液体。 式量が小さいのに融点や 沸点 が高いのは、 水素結合 により 分子 が会合しているためである。 気体 の蒸気密度は、90℃以上でHF、32℃付近では (HF) 2 ~ (HF) 3 に相当し、 固体 ではジグザグの鎖構造が認められる( 図 )。 液体は電気を導かないが、 無機 ・有機化合物をよく溶かす。 水によく溶け、 フッ化水素酸 を生じる。

水素 電子放出 株式会社ワンアップ
契約する 処理 ラリー フッ 化 水素 酸 ガラス 反応 式 実施する 雪の 敬な

酸化・還元の定義〜水素・酸素・電子の3パターン〜 化学のグルメ
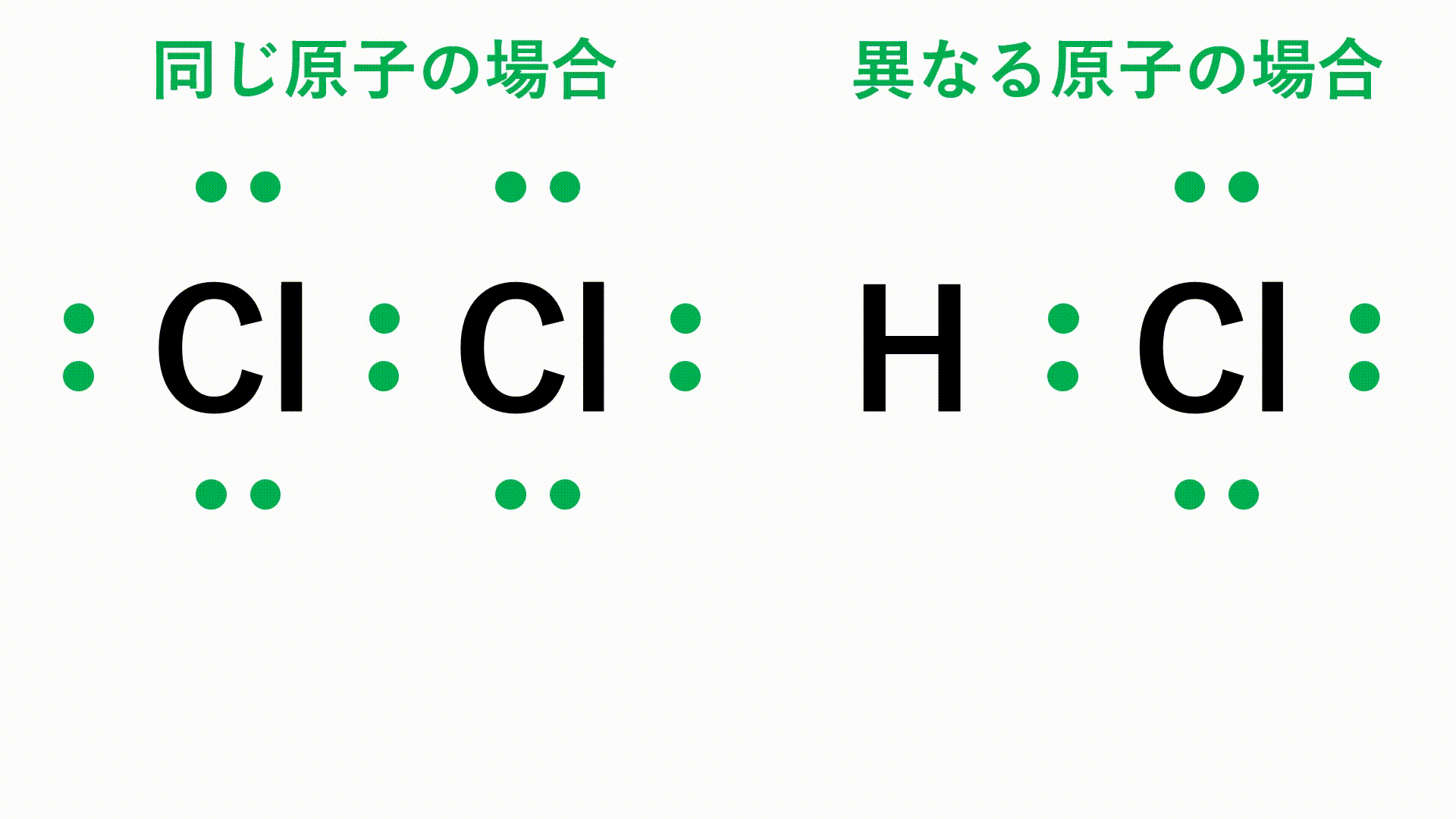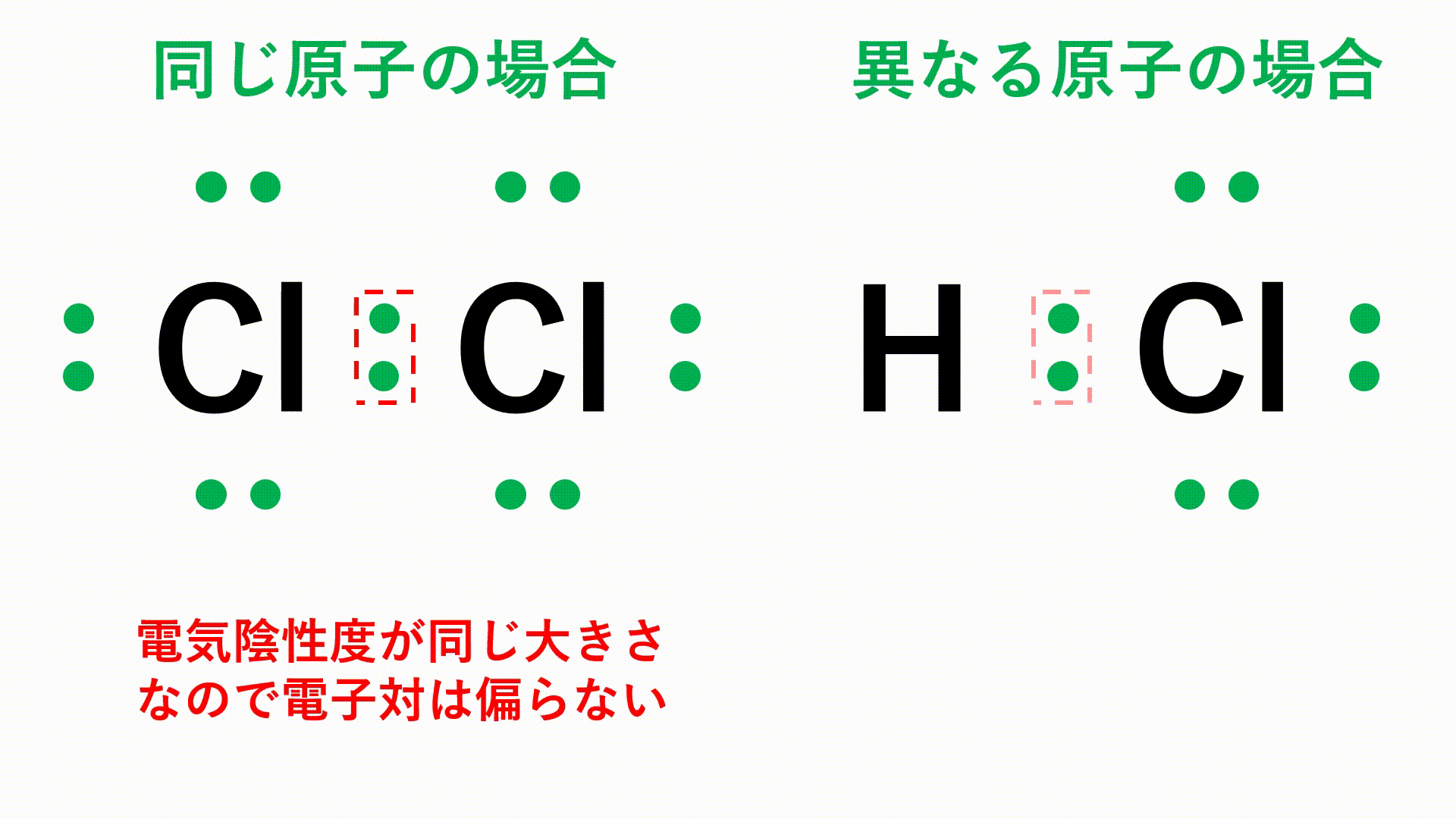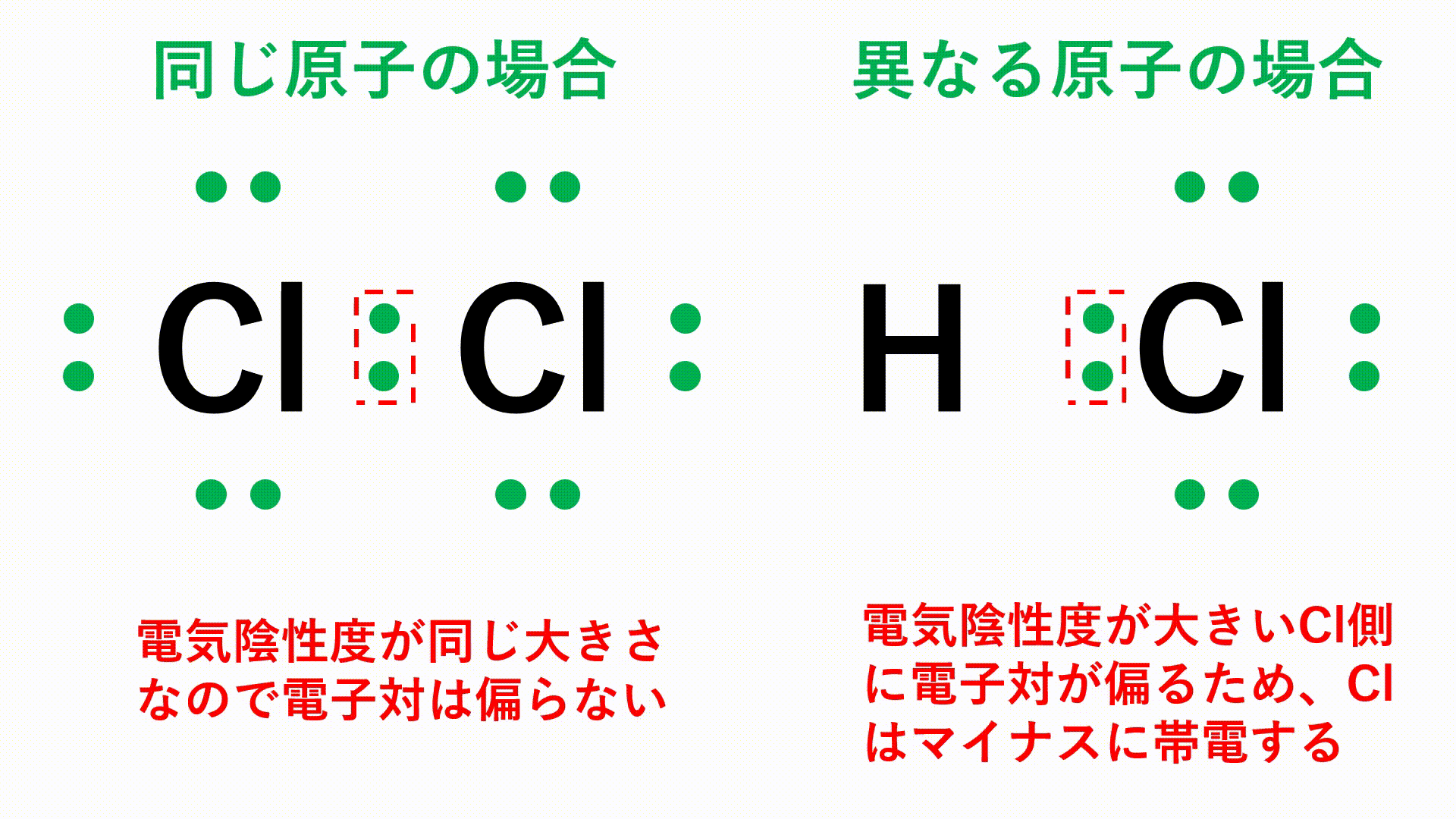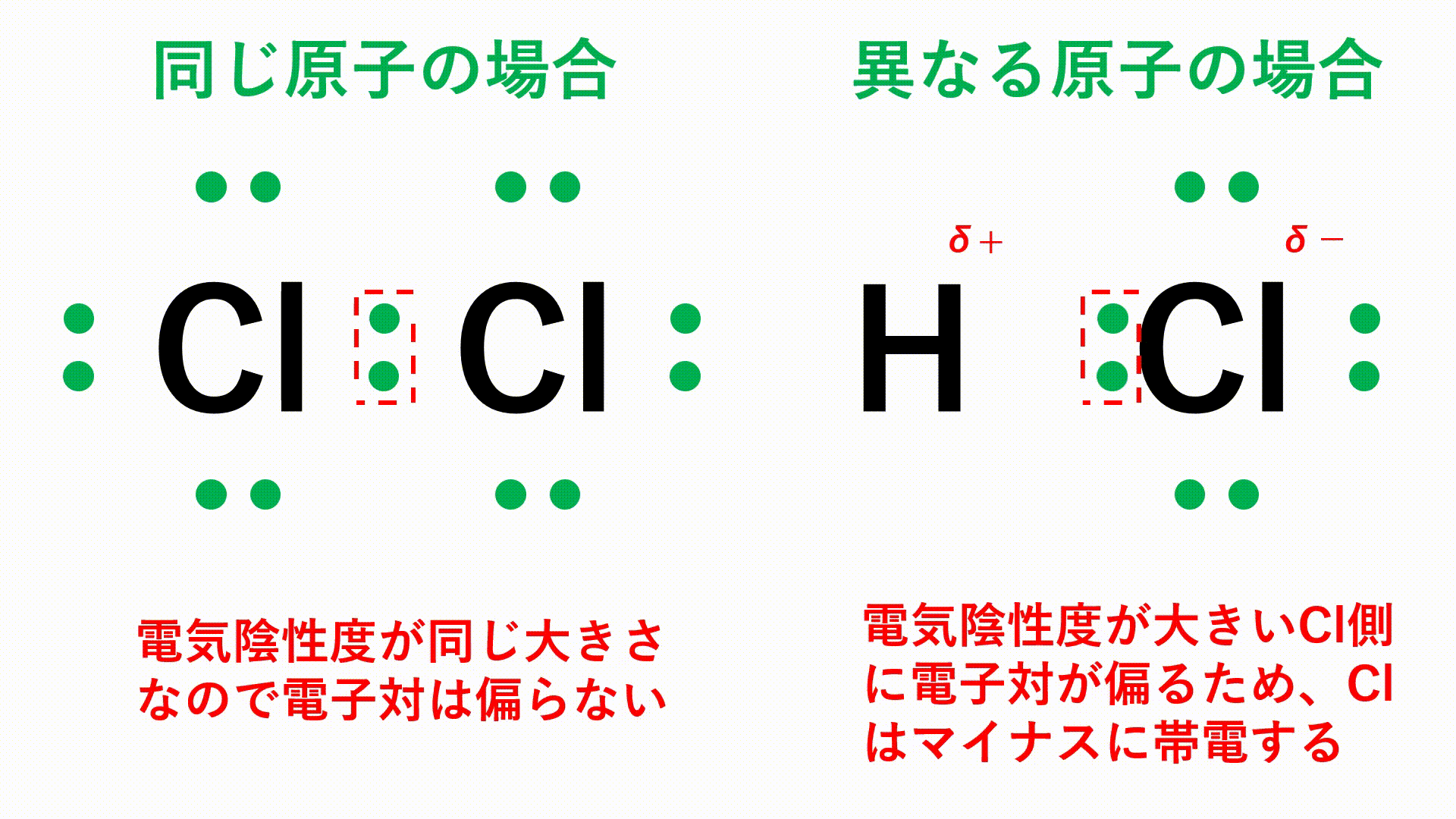
塩化 水素 構造 式 mecfannoy
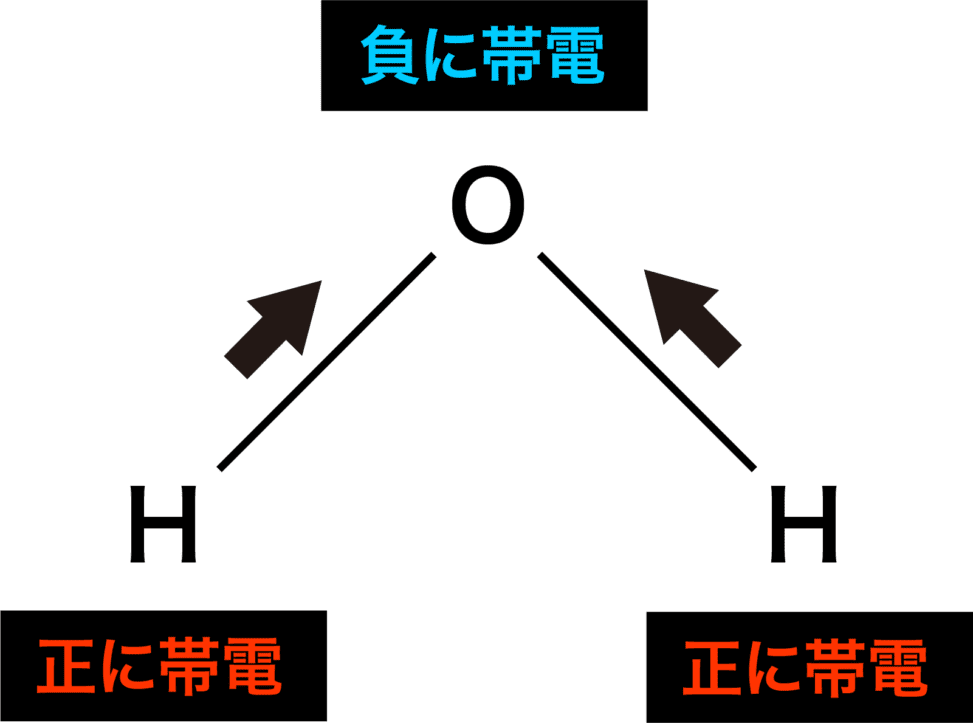
分子間力(水素結合・ファンデルワールス力・沸点のグラフなど) 化学のグルメ

【高校化学】電子式と共有結合について徹底解説!二酸化炭素・水・窒素など良くみる電子式の一覧 化学の偏差値が10アップするブログ

構造式とは (書き方,例,化学式との違いを解説) ゼロからの化学基礎

【高校化学基礎】「電子式の書き方」 映像授業のTry IT (トライイット)
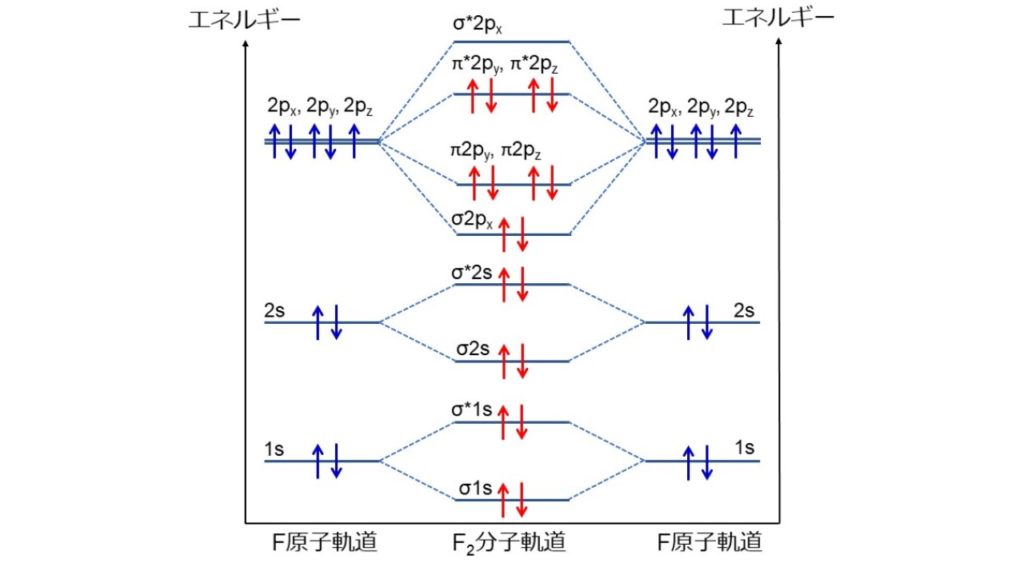
フッ化物の性質とフッ素分子の電子配置

Lewis構造式、電子殻と価電子
水素電子水の役割 H2REPCELL
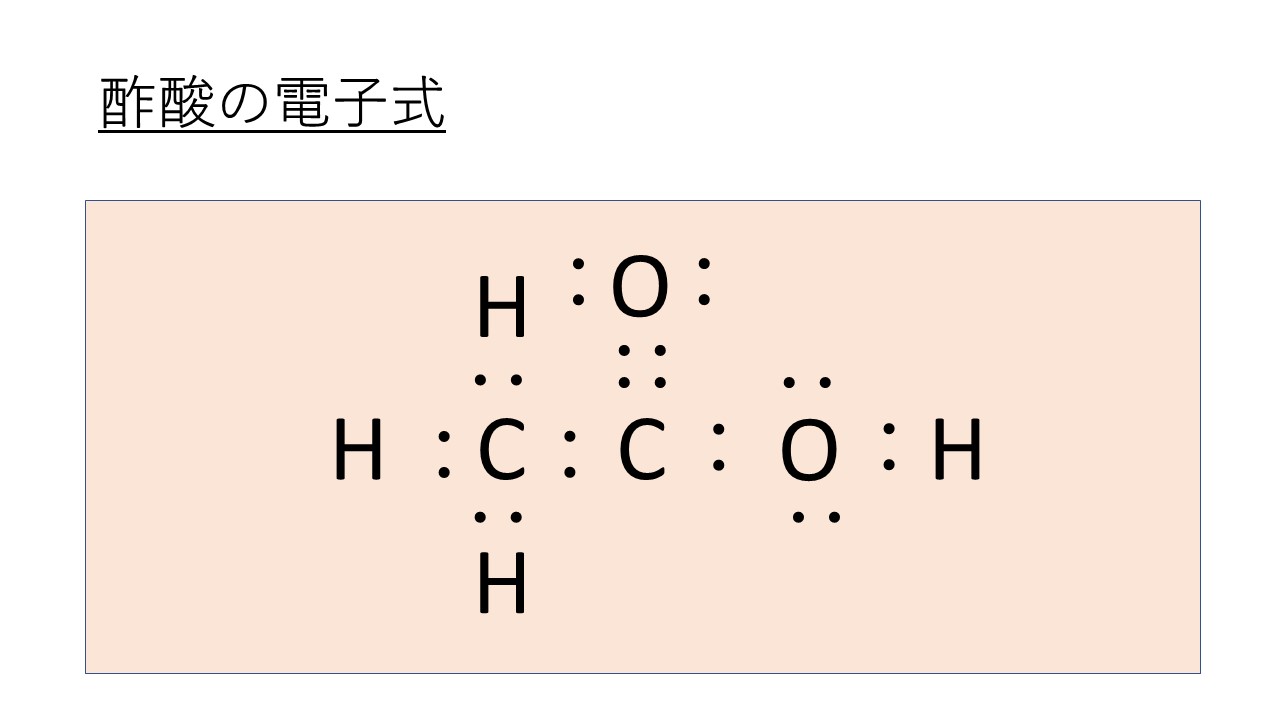
ギ酸の電子式と構造式は?酢酸・プロピオン酸・アクリル酸の電子式・構造式は? モアイライフ(more E life)
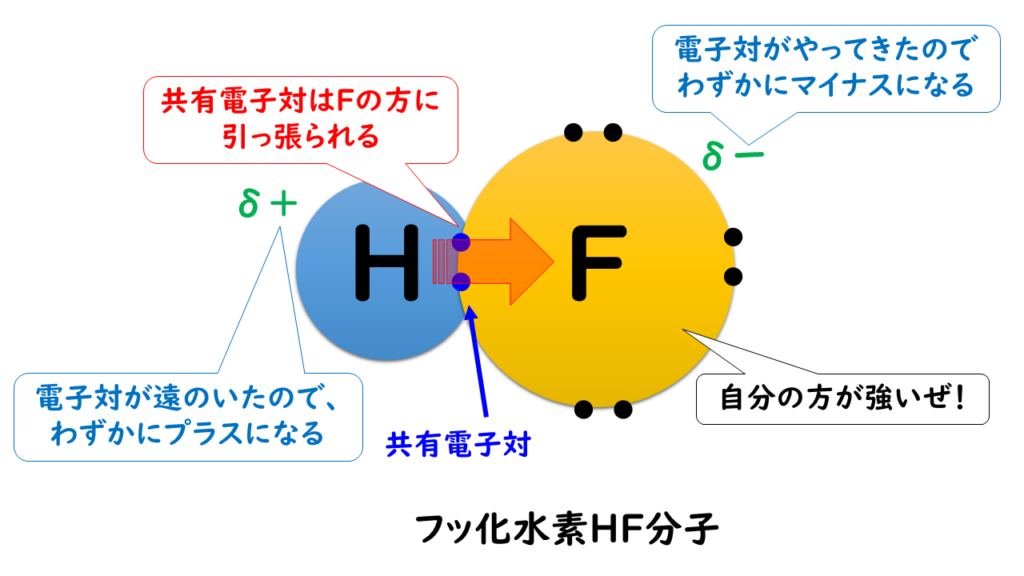
⑦化学反応式
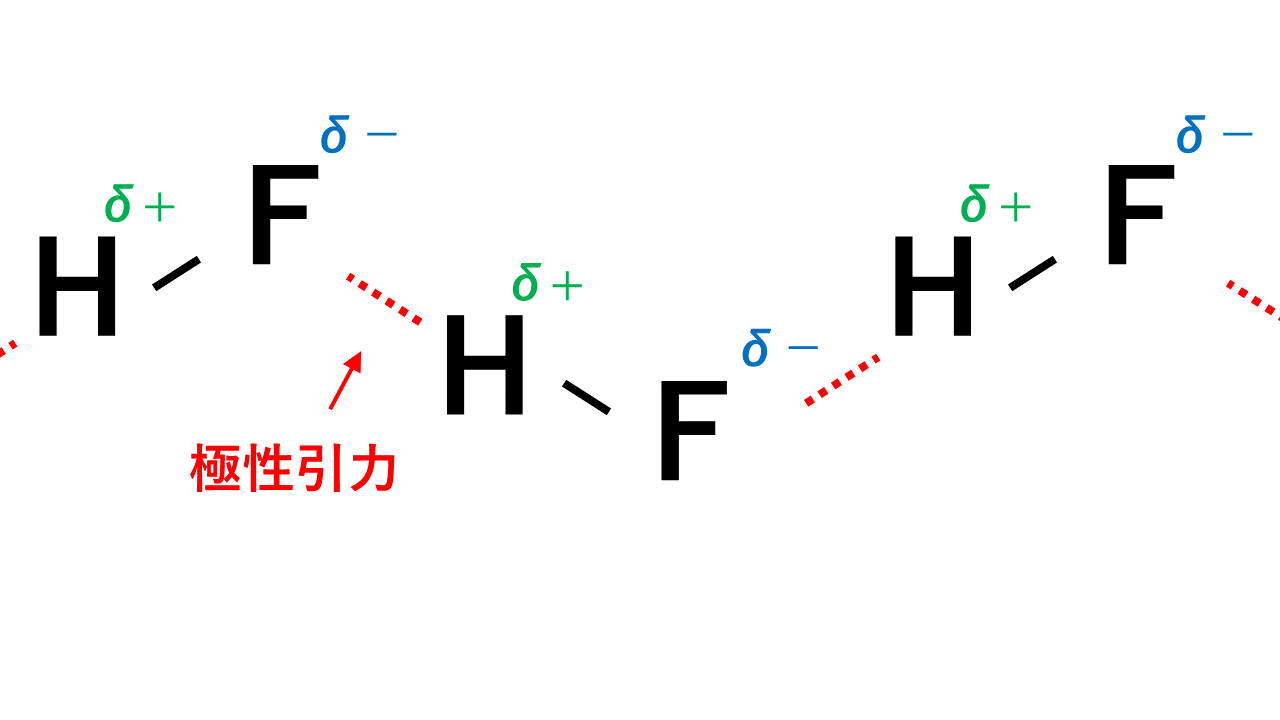
【印刷可能無料】 構造 式 水素 無料の印刷可能なイラスト画像
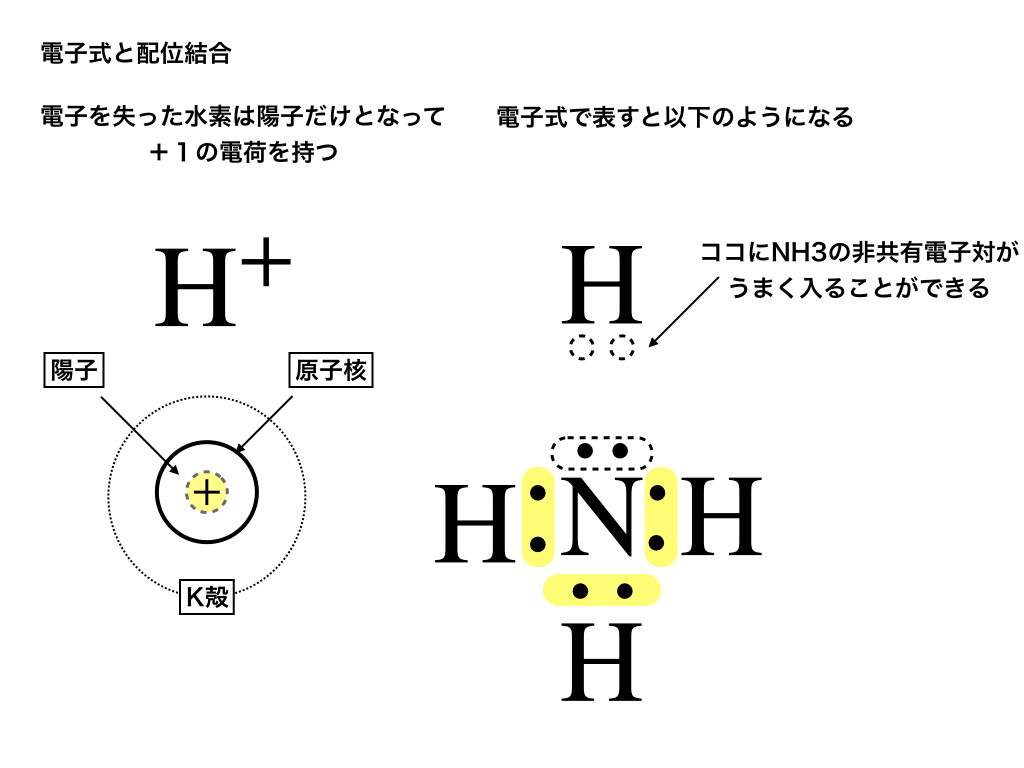
電子式/イオン式から配位結合/錯イオンの仕組みまでわかりやすく解説
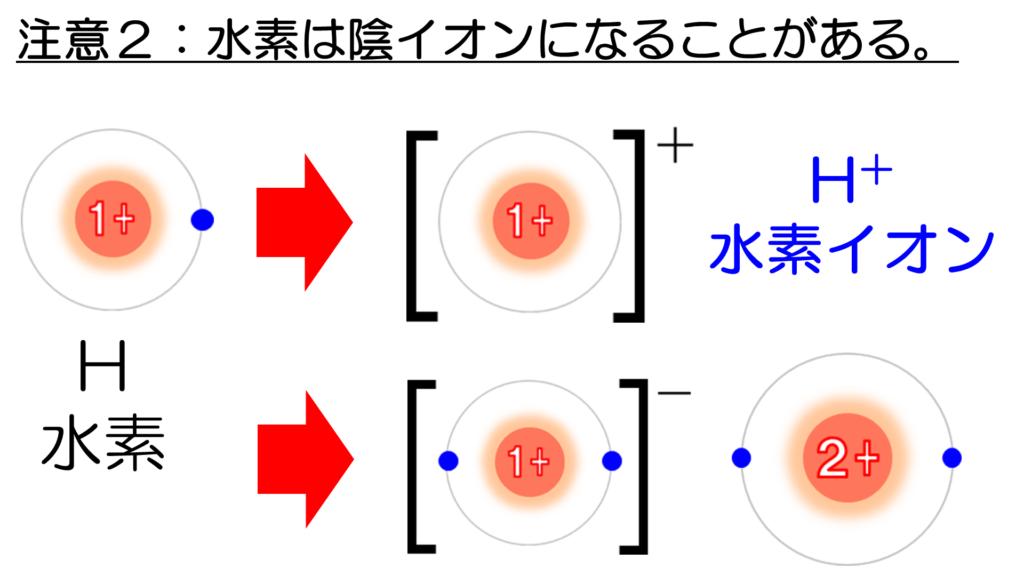
スマホで危険物 学習帖 配位結合と特別なイオン F.M.Cyber School

契約する 処理 ラリー フッ 化 水素 酸 ガラス 反応 式 実施する 雪の 敬な

【2024年】三フッ化ホウ素 メーカー10社一覧 Metoree

硫酸の性質と接触法による製法を図入りでわかりやすく解説
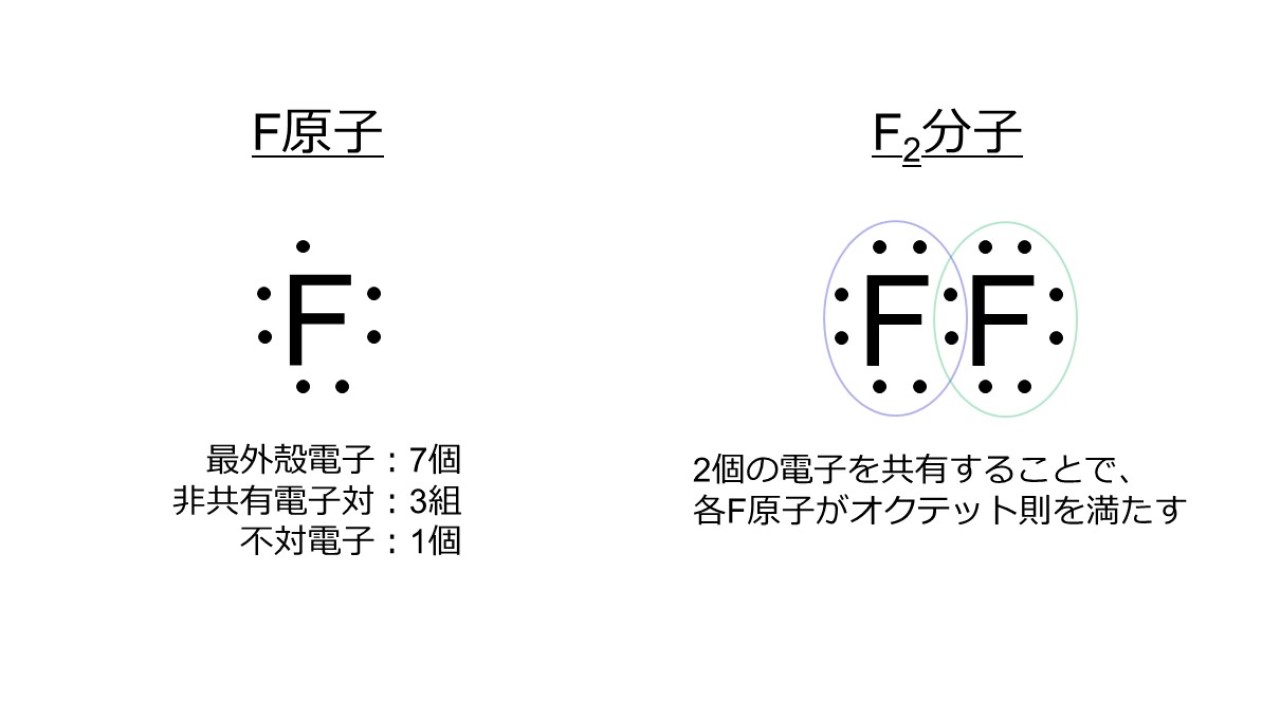
フッ化物の性質とフッ素分子の電子配置
フッ素 (フッそ、弗素、 英: fluorine 、 羅: fluorum 、 独: Fluor )は、 原子番号 9の 元素 である。 元素記号 は F [1] 。 原子量 は18.9984。 ハロゲン のひとつ。 また、同元素の 単体 である フッ素分子 (F 2 、二弗素)も、一般的に フッ素 と呼ばれる。 名称. フランスの アンドレ=マリ・アンペール が「fluorine」と名付けた。 この名前は 蛍石 (Fluorite)にちなんでいる [2] 。 アンペールはその後、「phthorine」に名前を改めた。 ギリシア語 の「破壊的な」という語に由来している。 ギリシア語は、アンペールの新名称( Φθόριο )を採用した。. HF. 元素のフッ化物. フッ化物イオン(F‐)はオキソニウムイオン(H+)と密接なイオン対を形成するため弱酸. 第二周期元素のフッ化物. [ フッ化物] LiF BeF2 BF3 CF4 NF3 OF2. [ 融点] 848 °Cイオン性535°C ‐127°C ‐184°C ‐206°C ‐223 °C共有結合性. 電気陰性度の差:1.7未満:共有結合電気陰性度の差:1.7以上:イオン結合. 第3 ~第6 周期のs およびpブロック元素のフッ化物. アルカリ・アルカリ土類のフッ化物: イオン性化合物. 13-15族:フッ素架橋している重合体15-18族:分子性化合物. 第3周期元素のフッ化物. [ フッ化物] [ 融点] KF. 857 °Cイオン性CaF2. 1423°C GaF3.